烷烃
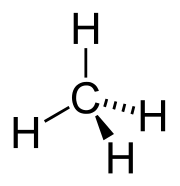
圖為最簡單的烷烴類:甲烷(CH4),僅由碳和氫組成,並且全由單鍵連接,符合烷烴類的特色。[1]
.mw-parser-output ruby>rt,.mw-parser-output ruby>rtc{font-feature-settings:"ruby"1}.mw-parser-output ruby.large{font-size:250%}.mw-parser-output ruby.larger{font-size:300%}.mw-parser-output ruby.large>rt,.mw-parser-output ruby.large>rtc{font-size:.3em}.mw-parser-output ruby.larger>rt,.mw-parser-output ruby.larger>rtc{font-size:.25em}
烷(wán)
烴(tīng)[2][3](英语:alkane),俗稱石蜡烃(paraffin)[4][5],是碳氫化合物下的一种饱和烃,其整体构造大多僅由碳、氢、碳-碳单键与碳氢单键所构成[6],同時也是最简单的一种有机化合物,而其下又可细分出链烷烃与环烷烃[7]。其名烷[8]是化学家取「碳」右下角的「火」,加上「完」造出的字,读音同「完」。「碳」表示其结构中含有碳,而「完」表示其分子结构中碳原子化合价完足的意思[9]。
目录
1 性質概論
2 物理性质
3 化学性质
3.1 燃燒反应
3.2 卤代反应
3.3 裂解反应
4 命名
4.1 鏈烷烴
4.2 環烷烴
4.2.1 具多環的環烷烴的命名法
4.3 特例
5 结构
6 異構體
6.1 链烷烴的異構體
7 分佈
7.1 太陽系的分布
7.2 地球上的分布
8 應用
8.1 工業上的應用
8.2 其他
9 注释
10 参考文献
11 延伸閱讀
12 外部链接
13 参见
性質概論
烷類皆難溶於水,在完全燃燒下可轉化為二氧化碳和水[10],反應式如下:
- CnH2n+2+3n+12 O2→n CO2+(n+1) H2O{displaystyle {rm {C_{n}H_{2n+2}+{frac {3n+1}{2}} O_{2}rightarrow n CO_{2}+(n+1) H_{2}O}}}
烷類會因組合結構的不同,其性質可能會有極大的差異。若結構相似,則性質相近;若結構不同,性質不同。[10] 正因此,烷類種類繁多;但也由此許多化學式相同的物質,其性質不相同。如戊烷(C5H12)[11]:
| 結構圖 | IUPAC命名 | 普通命名 | 熔點 | 沸點 |
|---|---|---|---|---|
| 戊烷 | 正戊烷 | -130℃[12] | 36℃[12] | |
 | 2-甲基丁烷 | 异戊烷 | -160℃[13] | 27.85℃[13] |
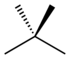 | 2,2-二甲基丙烷 | 新戊烷 | -19.5℃[14] | 9.5℃[14] |
物理性质

人工合成的正十二面體烷C20H20
烷烴有許多物理性質:
密度皆小於一。- 不溶于水,但溶于有机溶剂。
熔点與沸点随著分子量增大和碳链增长而升高,同碳数的烷烃,支链越多沸点越低。
一般情况下,碳数小于5的烷類(甲烷到丁烷)为气态,5-16之间的烷類(戊烷到十六烷)为液态,17个碳(十七烷)及以上的烷類为固态。[15]
烷烴 | 公式 | 沸點 [°C] | 熔點 [°C] | 20 °C下的狀態 | 密度 [g·cm3] |
甲烷 | CH4 | -162 | -182.5 | 氣體 | --- |
乙烷 | C2H6 | -89 | -182.8 | 氣體 | --- |
丙烷 | C3H8 | -42 | -187.7 | 氣體 | --- |
丁烷 | C4H10 | 0 | -138.0 | 氣體 | --- |
戊烷 | C5H12[16] | 35.2 [16] | -130 [16] | 液體 [16] | 0.649 [16] |
己烷 | C6H14 | 69 | -95 | 液體 | 0.659 |
庚烷 | C7H16[17] | 98.8 [17] | -91 [17] | 液體 [17] | 0.695 [17] |
辛烷 | C8H18[18] | 126 [18] | -57 [17] | 液體 [17] | 0.708 [17] |
壬烷 | C9H20[19] | 151.7 [19] | -53 [19] | 液體 [19] | 0.724 [19] |
癸烷 | C10H22[20] | 174.9 [20] | -30 [20] | 液體 [20] | 0.734 [20] |
十一烷 | C11H24[21] | 196.3 [21] | -26 [21] | 液體 [21] | 0.743 [21] |
十二烷 | C12H26[22] | 216 [22] | -12 [22] | 液體 [22] | 0.753 [22] |
十六烷 | C16H34 | 287 | 18 | 液体[23] | |
十七烷 | C17H36 | 302.2 | 22 | 固体 | 0.777[24] |
二十烷 | C20H42[25] | 343.4 [25] | 37 [25] | 固體 | 0.787 [25] |
三十烷 | C30H62 | 449.7 | 66 | 固體 | 0.810 |
四十烷 | C40H82 | 523.88 | 82 | 固體 | 0.817 |
五十烷 | C50H102 | 578.4 | 91 | 固體 | 0.824 |
化学性质
在正常情況下,烷烃性质很稳定,因为碳-氫键和碳-碳键相对稳定,难以断裂[26] 、以及烷烴不會搶奪官能團,所以不容易發生反應,除了下面三种反应,小分子的烷烃几乎不能进行其他反应。但支链多的烷烃,键角可能不同于arccos(−13){displaystyle arccos left(-{frac {1}{3}}right)}即109.5度,导致其容易發生反应。
燃燒反应
反應通式:R+O2→CO2+H2O{displaystyle {rm {R+O_{2}rightarrow CO_{2}+H_{2}O}}}[註 1]
所有的烷烃都能燃烧,而且反应放热极多[27]。烷烃完全燃烧生成CO2和H2O[10]。如果O2的量不足,就会产生有毒气体一氧化碳(CO),甚至炭黑(C)[28]。
以甲烷为例:
- CH4 + 2 O2 → CO2 + 2 H2O
O2供应不足时,反应如下:
- 2CH4 + 3 O2 → 2CO + 4 H2O
- CH4 + O2 → C + 2 H2O
分子量大的烷烃经常不能够完全燃烧,它们在燃烧时会有黑烟产生,就是炭黑。
卤代反应
反應通式:R+X2→RX+HX{displaystyle {rm {R+X_{2}rightarrow RX+HX}}}[註 2]
由于烷烃的结构太牢固,一般的有机反应不能进行。烷烃的卤代反应是一种自由基取代反应,反应的起始需要光能来产生自由基。
以下是甲烷被卤代的步骤。这个高度放热的反应可以引起爆炸。
- 链引发阶段:在紫外线的催化下形成两个Cl的自由基
- Cl2 → Cl* / *Cl
- 链增长阶段:一个H原子从甲烷中脱离;CH3Cl开始形成。
- CH4 + Cl* → CH3+ + HCl (慢)
- CH3+ + Cl2 → CH3Cl + Cl*
- 链终止阶段:两个自由基重新组合
- Cl* 和 Cl*, 或
- R* 和 Cl*, 或
- CH3* 和 CH3*.[29]
裂解反应
裂化反应是大分子烃在高温、高压或有催化剂的条件下,分裂成小分子烃的过程。裂化反应属于消除反应,因此烷烃的裂化总是生成烯烃。如十六烷(C16H34)经裂化可得到辛烷(C8H18)和辛烯(C8H16)。
由于每个键的环境不同,断裂的机率也就不同,下面以丁烷的裂化为例讨论这一点:
- CH3-CH2-CH2-CH3 → CH4 + CH2=CH-CH3
- 过程中CH3-CH2键断裂,可能性为48%;
- CH3-CH2-CH2-CH3 → CH3-CH3 + CH2=CH2
- 过程中CH2-CH2键断裂,可能性为38%;
- CH3-CH2-CH2-CH3 → CH2=CH-CH2-CH3 + H2
- 过程中C-H键断裂,可能性为14%。[29]
- 过程中C-H键断裂,可能性为14%。[29]
裂化反应中,不同的条件能引发不同的机理,但反应过程类似。热分解过程中有碳自由基产生,催化裂化过程中产生碳正离子和氢负离子。这些极不稳定的中间体经过重排、键的断裂、氢的转移等步骤形成稳定的小分子烃。
在工业中,深度的裂化叫做裂解,裂解的产物都是气体,称为裂解气。
命名
烷類的命名多採IUPAC命名法。
命名烷類的首要步驟是分析其為環狀亦或是鏈狀,再進行命名步驟。[30]
鏈烷烴
化學通式:CnH2n+2[31]
鏈烷烴的命名步驟為:
- 找出最長的碳鏈當主鏈,依碳數命名主鏈,前十個以天干[註 3]代表碳數,碳數多於十個時,以中文數字命名,如:十一烷。
- 從最近的取代基位置編號:1、2、3...(使取代基的位置數字越小越好)。以數字代表取代基的位置。數字與中文數字之間以 - 隔開。
- 有多個取代基時,以取代基數字最小且最長的碳鏈當主鏈,並依甲基、乙基、丙基的順序列出所有取代基。
- 有兩個以上的取代基相同時,在取代基前面加入中文數字:一、二、三...,如:二甲基,其位置以“,”(逗号)隔開,一起列於取代基前面。
因為烷類一般簡單,故亦會使用「正、異、新」去區隔同樣化學式的烷類。IUPAC也曾推薦過此種命名方式[32]。例如己烷命名方式:
普通命名 | IUPAC命名 | 结构简式 | 结构式 |
|---|---|---|---|
己烷、 正己烷 | 己烷 | CH3(CH2)4CH3 | |
异己烷 | 2-甲基戊烷 | (CH3)2CH(CH2)2CH3 | 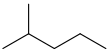 [34] [34] |
新己烷 | 2,2-二甲基丁烷 | CH3C(CH3)2CH2CH3 | 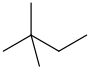 [35] [35] |
環烷烴
化學通式:CnH2(n+1-g)[註 4]
簡單的環烷烴的命名方式基本上和烷類方式相同,僅需在前添加一環字,以做識別。例如環丙烷:

環丙烷,化學式為C3H6[36]
具多環的環烷烴的命名法
除非有俗名,否則具多環的環烷烴如桥环烷烴及螺环烷烴的命名較為複雜。名字包括表示環數量的前綴(如「二環」)、各環內碳原子總數的後綴以及表示各端點之間碳原子數的數字前綴(表示於中括號內。多個環公用的碳原子,即橋頭碳不計入內)。
如例一、例二:

例一,二环[3.2.0]庚烷。

例二,雙環[2.2.1]庚烷(俗稱降冰片烷)
這個環烷總碳數為七,由兩個環組成,尾為「庚烷」,頭為「雙環」。兩個被共用的碳原子間有三個連接路線:一為五元環的部分,共三個碳(兩個橋頭碳不計入內,下同);二為四元環的部分,共二個碳;三為兩環之間共用的邊綫,只由兩橋頭碳直接連結,中間沒有碳。由此得出中括號內的數字(以降序表示數字之間用點分隔),[3.2.0]。故上圖的環烷名為二环[3.2.0]庚烷,而數字的個數總比環數多一個(在此有兩個環及三個數字)。「[3.2.0]二环庚烷」亦可接受,但環上有取代基時「二环[3.2.0]庚烷」有保留前面的位置的好處,方便加上其他含數字的前綴,以符合IUPAC命名常規。
上圖環烷總碳數為七,全為單鍵,詞尾為庚烷;兩共用碳間有兩對二碳碳鏈,也被一個碳原子連接著,故詞尾之前的數字前綴為[2,2,1](共用碳不計入內);這個環烷由兩個環組成,故前綴為「雙環」,最後得出「雙環[2.2.1]庚烷」。
特例
出于化工习惯,异辛烷不是2-甲基庚烷,而是2,2,4-三甲基戊烷。
结构
烷烃中,每个碳原子都是四价的,采用sp3杂化轨道,与周围的4个碳或氢原子形成牢固的σ键,可以旋轉,故烷類無順反異構物。
为了使键的排斥力最小,连接在同一个碳上的四个原子形成四面体。甲烷是标准的正四面体形态,其键角为arccos(−13){displaystyle arccos left(-{frac {1}{3}}right)},大約等於109°28′。[37]
下面是前10种直链烷烃的分子式和结构模型图。
|
|
異構體
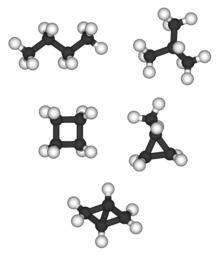
不同的四碳烴類(從左到右): 正丁烷和异丁烷為同分異構體,化學式皆為C4H10[38];環丁烷和异丁烯為同分異構體,化學式皆為C4H8
雙環[1.1.0]丁烷是唯一化學式為C4H6的烷烴。
烷類的異構物大多鏈異構(由於支鏈不同而造成的異構物)。超过3个碳原子的烷烃可以以多种方式排列,形成同分异构体。烷烴異構物的數目會隨著碳數增加而增加(OEIS中的数列A000602)[39]。
链烷烴的異構體
- C1:沒有同分異構體: 甲烷
- C2:沒有同分異構體: 乙烷
- C3:沒有同分異構體: 丙烷
- C4:兩個異構體: 正丁烷, 異丁烷
- C5:三個異構體: 正戊烷, 異戊烷, 新戊烷
- C6:五個異構體: 己烷
- C12:三百五十五個異構體
- C32: 27,711,253,769個異構體
- C60: 22,158,734,535,770,411,074,184個異構體,其中有很多為非穩定狀態。[40]
分佈

烷烴是木星大氣層的主要成分[41]
烷烴在宇宙間分布眾多,其中分布最多的是甲烷,而極少見由50個碳原子以上所構成的烷烴[42]。
太陽系的分布
烷烴分布於太陽系間許多星球的大氣層。有些佔了較多的比例,例如天王星(2.3%)[43]、土衛六(5%)[44],但在大多星球上,分布較少,如地球、火星、土星等等[45]。
地球上的分布
地球上的烷烴多為甲烷,而甲烷的濃度隨地球緯度降低而遞減,並在北緯40度及赤道附近都有明顯濃度下降。北半球與南半球平均濃度各為1.65ppm及1.55ppm。[46]
應用
工業上的應用
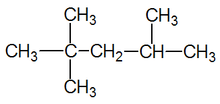
异辛烷(2,2,4-三甲基戊烷)的结构式。
由于烷烃的制取成本较高(一般要用烯烃催化加氢),所以在工业上不制取烷烃,而是直接从石油中提取。由于烷烃不易发生反应,所以工业上也不把它作为化工基本原料。烷烃的作用主要是做燃料。天然气和沼气(主要成分为甲烷)是近来广泛使用的清洁能源。
由於烷烴大多來自於石油,所以必須經過分馏的過程,以得到各種不同用途的烷烴類。
分餾結果大約如下:
| 成分 | 碳數 | 分餾溫度 | 用途 |
|---|---|---|---|
| 石油氣 | C1–C4 | <20℃ | 燃料、化工原料 |
| 石油醚 | C5–C6 | 20℃-60℃ | 有機溶劑 |
| 汽油 | C7–C9 | 60℃-200℃ | 燃料 |
| 煤油 | C10–C16 | 175℃-300℃ | 燃料 |
| 柴油 | C15–C20 | 250℃-400℃ | 燃料 |
- C20以上的馏分成分是重油,再经减压蒸馏能得到润滑油、沥青等物质。[47]
其他
异辛烷與庚烷是汽油抗爆震度的一个标准,其辛烷值定为100與0。[48][49][50]
注释
^ R即為烷烴。
^ X即為鹵素。
^ 十天干:甲、乙、丙、丁、戊、己、庚、辛、壬、癸
^ n為碳原子數,g為環的數量。
参考文献
^ 国二下自然与生活科技(康軒版), 第四冊. 第四章. 有機化合物. (PDF). [2011-10-04].
^ 《化學命名原則》,第四版,國立編譯館,2004
^ 中華民國教育部重編國語辭典修訂本 - 烴
^ 化工词典上的烷烃. ChemYQ.com. [2011-10-04].
^ 台灣銀行/金融小百科/景氣循環產業/塑化/石蠟烴解釋頁. 嘉實資訊. [2011-10-04].
^ http://chem188.cn/Article/ShowArticle.asp?ArticleID=3409,其中亦有可能出现卤素,因为其价数和氢原子相同,为+1,所以可以取代氢原子。
^ 分類 (PDF). Docs.google.com. [2017-08-17].
^ 烷的解释|烷的意思|汉典“烷”字的基本解释. Zdic.net. [2017-08-17].
^ http://dict.revised.moe.edu.tw/cgi-bin/cbdic/gsweb.cgi?o=dcbdic&searchid=W00000011486. [2017-08-17]. 缺少或|title=为空 (帮助)
^ 10.010.110.2 許立侖、許喆翔. 《國中自然與生活科技 第四冊學習講義》P138. 康軒文教事業.
^ 异戊烷
^ 12.012.1 正戊烷 | 109-66-0. Chemicalbook.com. [2017-08-17].
^ 13.013.1 2-甲基丁烷(异戊烷) CAS#: 78-78-4. Chemicalbook.com. [2017-08-17].
^ 14.014.1 新戊烷(463-82-1) MSDS 性质 熔点 处理 密度 比重. Chemicalbook.com. [2017-08-17].
^ 參考資料. Docs.google.com. [2017-08-17].
^ 16.016.116.216.316.4 戊烷. 化工百科. [2015-05-28].
^ 17.017.117.217.317.417.517.617.7 庚烷. 化工百科. [2015-05-28].
^ 18.018.1 辛烷. 化工百科. [2015-05-28].
^ 19.019.119.219.319.4 壬烷. 化工百科. [2015-05-28].
^ 20.020.120.220.320.4 癸烷. 化工百科. [2015-05-28].
^ 21.021.121.221.321.4 十一烷. 化工百科. [2015-05-28].
^ 22.022.122.222.322.4 十二烷. 化工百科. [2015-05-28].
^ Record in the GESTIS Substance Database from the IFA
^ she., Ren min jiao yu chu ban; 人民教育出版社. Hua xue (bi xiu). 2. Di 1 ban. Beijing: Ren min jiao yu chu ban she https://www.worldcat.org/oclc/666543370. 2004. ISBN 9787107176494. OCLC 666543370. 缺少或|title=为空 (帮助)
^ 25.025.125.225.3 二十烷. 化工百科. [2015-05-28].
^ 冀政勤、毛翰梅. 有機化學. 台北市: 五南. 2001-02-22. ISBN 957-11-2276-9.
^ 學習加油站遷移轉址到教育雲-教育大市集. Content.edu.tw. [2017-08-17].
^ 烷類(Alkanes)(二)──化學反應 | 科學Online. Highscope.ch.ntu.edu.tw. 2014-06-20 [2017-08-17].
^ 29.029.1 https://docs.google.com/viewer?a=v&q=cache:UylIK0hlBXMJ:163.23.148.7/sweb/pub/downfiles.php%3Frec_id%3D176%26rel_nm%3D1%26account%3Djiahui+%E7%83%B7%E9%A1%9E+%E7%87%83%E7%87%92&hl=zh-TW&gl=tw&pid=bl&srcid=ADGEESjVn_S4UBj386pOI7NtQloiuyGfCymgttRAfWW2AE_PJB9awjuKFypwR0q1w3QyFOwcCqsao9NApFyloGNUquPoILBB4iZ2ZHgi_DLolYLdP7zuIRY4qYXTKkczeEWQbTLiXZv4&sig=AHIEtbTaNJ-0RUBSkexAGhzfaapV4QNrZQ. [2017-08-17]. 缺少或|title=为空 (帮助)
^ 參考自IUPAC命名法
^ Silderberg, 623
^ Panico, R.; Powell, W. H. (编). A Guide to IUPAC Nomenclature of Organic Compounds 1993. Oxford: Blackwell Science. 1994. ISBN 978-0-632-03488-8.
^ 己烷;物理性质,化学性质,英文名,分子量,结构式,分子式,CAS号,制备方法,用途,溶点,沸点,毒性,MSDS,供应商,公司. Chemyq.com. 2014-10-01 [2017-08-17].
^ 异己烷;2-Methylpentane;Isohexane;物理性质,化学性质,英文名,分子量,结构式,分子式,CAS号,制备方法,用途,溶点,沸点,毒性,MSDS,供应商,公司. Chemyq.com. 2014-10-01 [2017-08-17].
^ CAS 登录号:75-83-2, 2,2-二甲基丁烷, 新己烷. Chemblink.com. [2017-08-17].
^ Merck Index, 11th Edition, 2755.
^ [1][失效連結]
^ Bond dissociation energies: Senosiain, J. P.; Han, J. H.; Musgrave, C. B.; Golden, D. M. Faraday Discussions (2001), vol. 119, 173-189
^ 學習加油站遷移轉址到教育雲-教育大市集. Content.edu.tw. [2017-08-17].
^ Meierhenrich, U. Amino Acids and the Asymmetry of Life. Springer. 2008 [18 October 2008]. ISBN 978-3-540-76885-2.
^ Kim, S. J.; Caldwell, J.; Rivolo, A. R.; Wagner, R. Infrared Polar Brightening on Jupiter III. Spectrometry from the Voyager 1 IRIS Experiment. Icarus. 1985, 64: 233–48 [2007-08-28]. doi:10.1016/0019-1035(85)90201-5.
^ 烷的意思.含义.解释.读音.在线高级汉语词典查询. Chinabaike.com. [2017-08-17].
^ 存档副本. [2011-09-15]. (原始内容存档于2010-09-06).
^ http://www.natureasia.com/taiwan/nature/updates/index.php?i=5857&issue=7080[永久失效連結]
^ Courtin, R.; Gautier, D.; Marten, A.; Bezard, B. The Composition of Saturn's Atmosphere at Temperate Northern Latitudes from Voyager IRIS spectra. Bulletin of the American Astronomical Society. 1967, 15: 831 [2007-02-04].
^ http://210.60.226.25/science/content/1986/00110203/0010.htm[永久失效連結]
^ 石油分餾產品的沸點與成分. Emfuel.com. [2017-08-17].
^ Petroleum and Coal. Chemed.chem.purdue.edu. [2017-08-17].
^ (PDF) http://www.iupac.org/publications/pac/1983/pdf/5502x0199.pdf. [2017-08-17]. 缺少或|title=为空 (帮助)
^ 存档副本. [2015-05-15]. (原始内容存档于2015-04-07).
延伸閱讀
.mw-parser-output .refbegin{font-size:90%;margin-bottom:0.5em}.mw-parser-output .refbegin-hanging-indents>ul{list-style-type:none;margin-left:0}.mw-parser-output .refbegin-hanging-indents>ul>li,.mw-parser-output .refbegin-hanging-indents>dl>dd{margin-left:0;padding-left:3.2em;text-indent:-3.2em;list-style:none}.mw-parser-output .refbegin-100{font-size:100%}
- Virtual Textbook of Organic Chemistry
外部链接
维基共享资源中相关的多媒体资源:Alkane |
| 查询維基詞典中的烷烃。 |
参见
- 环烷烃
烯烃 - 炔烃
- 烷基
- 官能团
- 裂化
- 烴
| ||||||||||||||||||||||
| |||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
|













